Lewis Saeure Beispiel

Beispiele für lewis säuren 1.
Lewis saeure beispiel. B ch 3 3 b oh 3 bf 3 alcl 3. Die folgende liste zeigt eine auswahl von säuren aufgelistet sind der gebräuchliche trivialname. Mit dem säure begriff nach lewis ist es möglich die sauren eigenschaften von stoffen zu erklären die keine protonendonatoren nach brønsted sind. Als beispiel kann aluminiumchlorid dienen das in wasser sauer reagiert obwohl es keinen wasserstoff enthält.
Verallgemeinerung der obigen regel. Typische lewis basen sind z b. Lewis basen treten als typische liganden in metallkomplexen auf siehe auch komplexchemie. Zncl2 sc otf 3oder bf3 oet2 vermitteln die pd katalysierte arylierung von methylpyridinen und ähnlichen heterocyclen siehe beispiel.
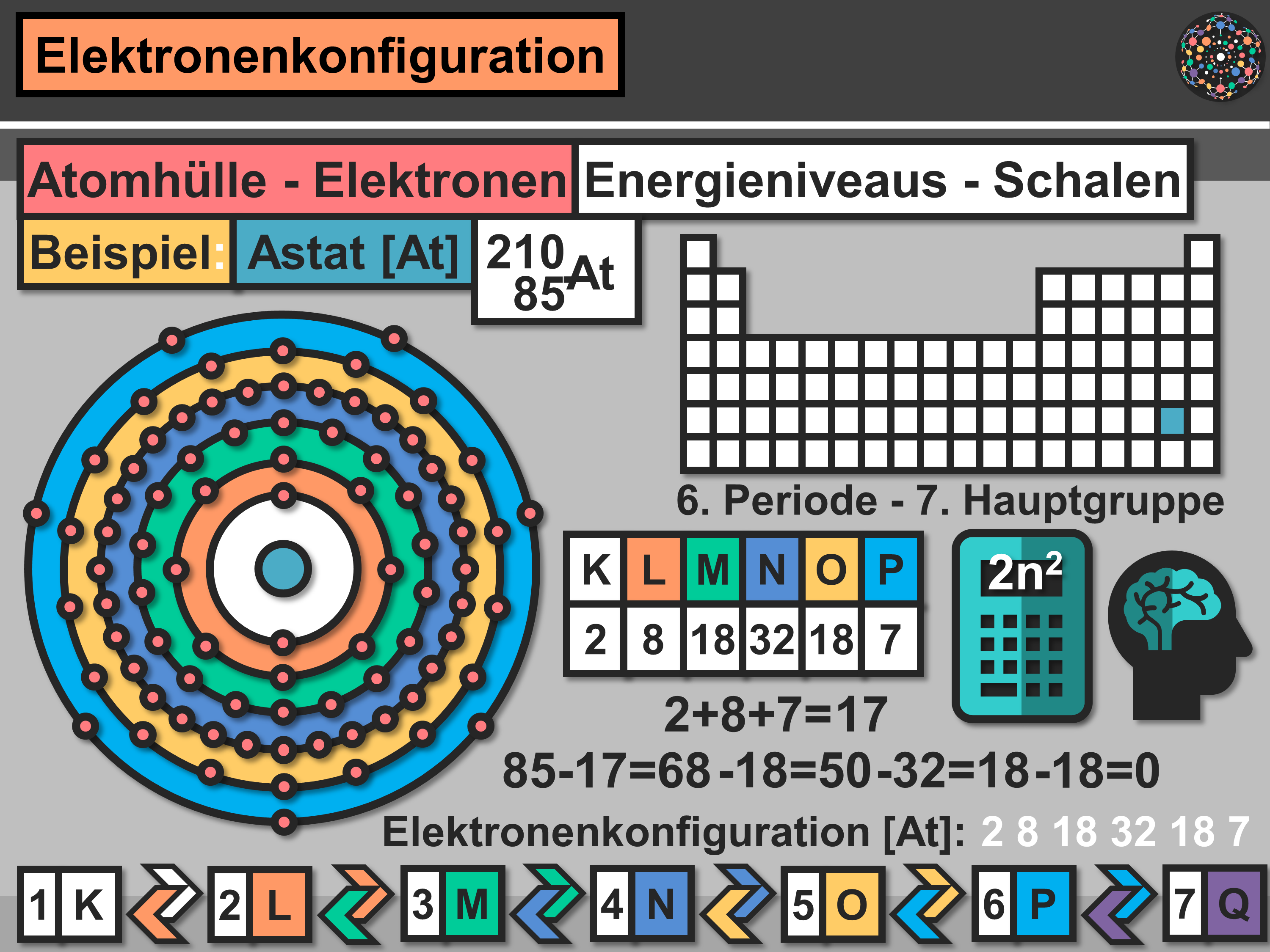
Verbindungen in denen ein atom keine edelgaskonfiguration hat. Nh 3 h 2 o f cn oder co. English i ve known you and i know lewis deep down right deep down here that you are going to make this swim. Moleküle oder atome mit unvollständigem elektronenoktett wie bf 3 alcl 3 oder das schwefel atom sind typische lewis säuren.
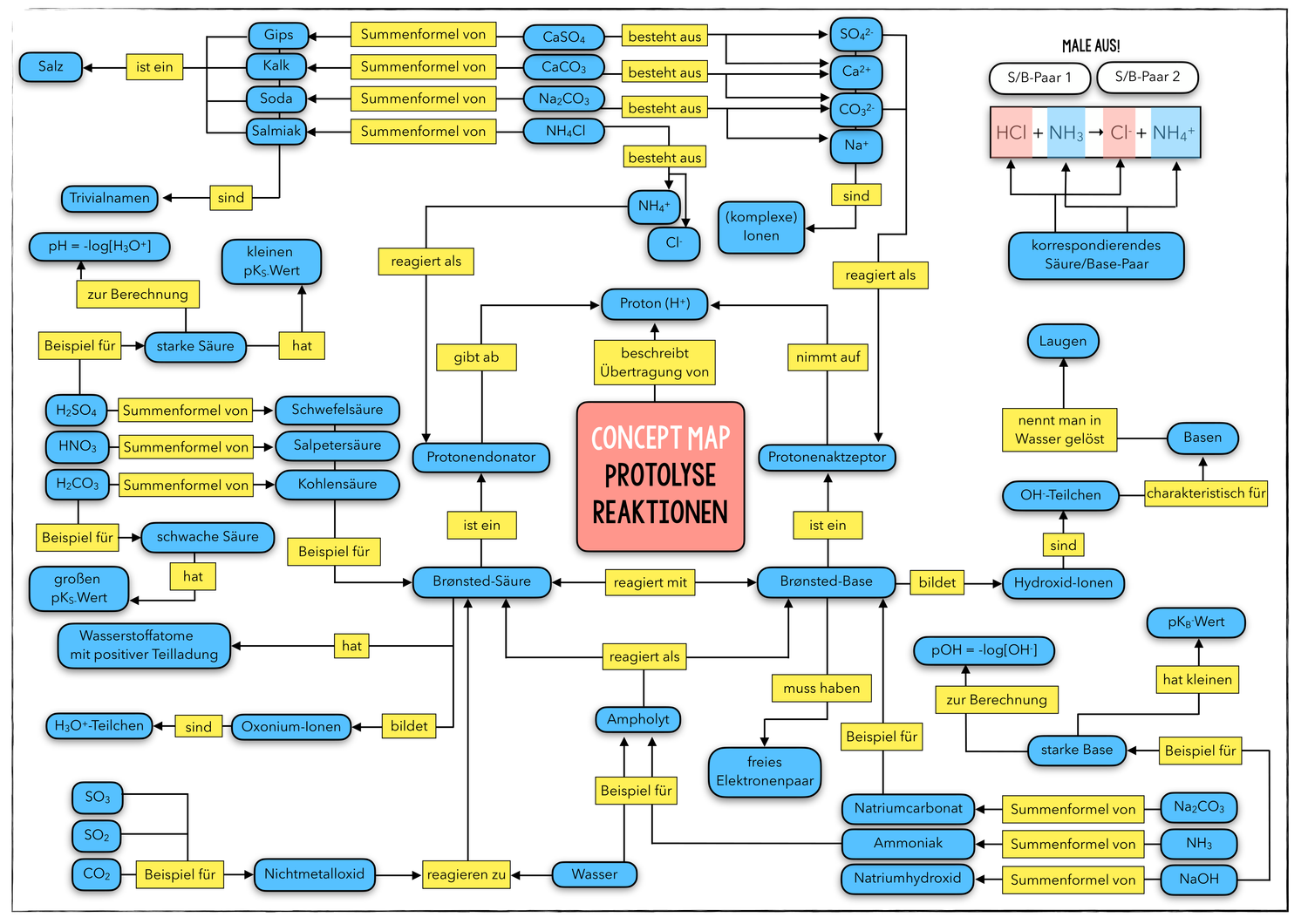
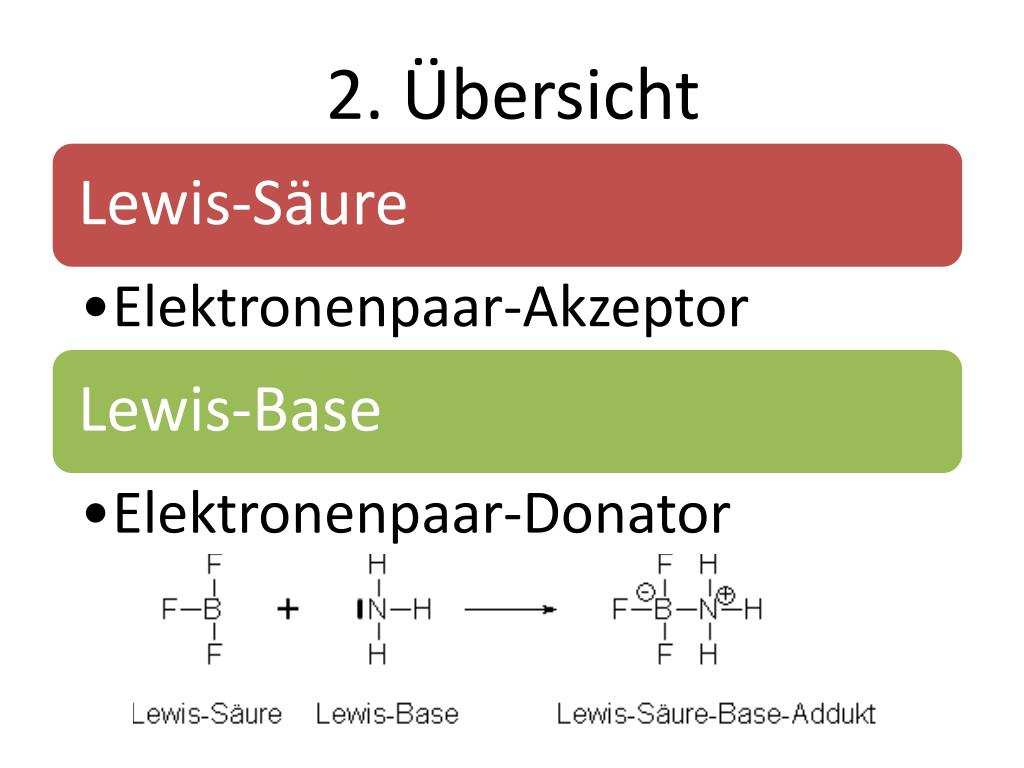
Die komplexierung des stickstoffatoms im heterocyclus. Reaktion von bortrifluorid und ammoniak ammoniak reagiert mit bortrifluorid einer verbindung mit unvollständigem elektronenok tett indem eine bindung durch das freie elektronenpaar des ammoniaks ausgebildet wird. Verbindungen mit atomen ohne edelgaskonfiguration z b. Die lewis base ist der ligand der sein elektronenpaar für eine bindung zur verfügung stellt besondere eigenschaft.
Verbindungen mit unvollständigem oder instabilem elektronenoktett wie. Die liste erhebt keinen anspruch auf vollständigkeit. Das produkt der reaktion einer lewis säure mit einer lewis base kann als lewis säure base addukt koordinationsverbindung oder auch als akzeptor donator komplex bezeichnet werden. Komplexbildung als beispiel für lewis säure base reaktionen die lewis säure ist das zentralteilchen zumeist ein kation mn besondere eigenschaft.
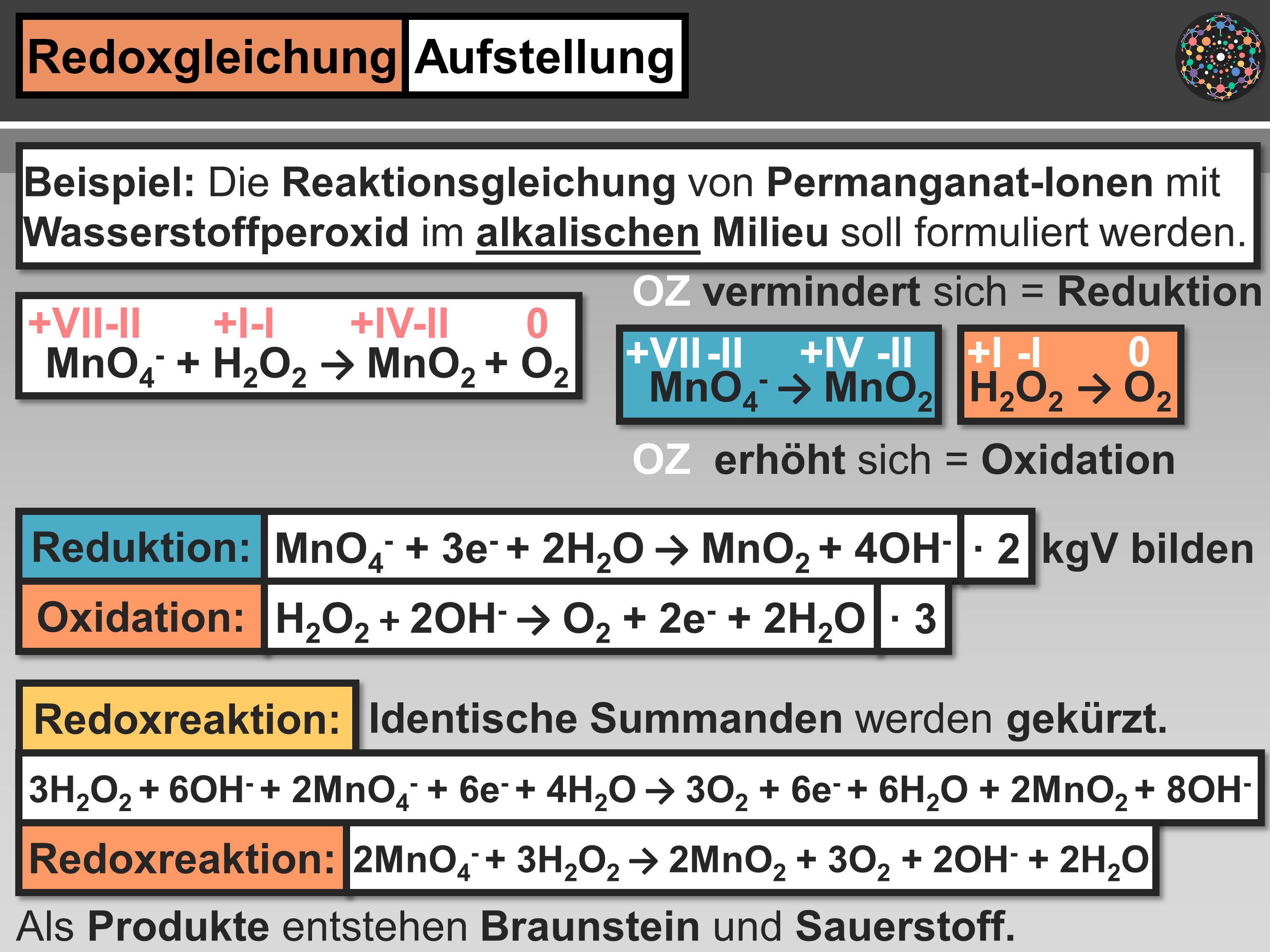
Eine lewis säure ist ein elektrophiler elektronenpaarakzeptor kann also elektronenpaare anlagern. Hier erweitert lewis das konzept. Im gegensatz dazu ist eine lewis base ein elektronenpaardonator mit freien elektronenpaaren die einer lewis säure zur bindung zur verfügung gestellt werden können. Zu den lewis säuren zählen.
Der iupac name die offizielle bezeichnung.